“影响化学反应速率的因素”教学设计
上海市第十中学 王艺扉
一、单元内容分析
1. 单元简介
本单元“化学反应速率和化学平衡”,出自上海科学技术出版社化学必修二教材第六章。本单元包括化学反应速率、化学平衡、化工生产。
2. 单元目标
本单元内容与《普通高中化学课程标准(2017年版2020 年修订)》(以下简称《课程标准》)“课程内容——必修课程”板块中的“主题 3:物质结构基础与化学反应规律”“主题 2:常见的无机物及其应用”直接对应, 具体对应主题 3“化学反应的限度和快慢”“学生必做实验”,以及主题 2“非金属及其化合物”“物质性质及物质转化的价值”四个部分的内容。本单元的具体内容要求和学业要求见表1。
表 1 “化学反应速率和化学平衡”单元内容要求与学业要求
|
内容要求 |
学业要求 |
|
|
化学反应的 限度和快慢 |
体会从限度和快慢两个方面去认识和 调控化学反应的重要性。了解可逆反应 的含义,知道可逆反应在一定条件下能 达到化学平衡。知道化学反应平均速率 的表示方法,通过实验探究影响化学反 应速率的因素。认识化学变化时有条件 的,学习运用变量控制方法研究化学反 应,了解控制反应条件在生产和科学研 究中的作用。 |
1 能从化学反应限度和快慢的角度解释生产、生活中简单的化学现象。 2 能描述化学平衡状态,判断化学反应是否达到平衡。 3 能运用变量控制的方法探究影响化学反应速率的因素,能初步解释化学实验和化工生产中反应条件的选择问题。 |
|
非金属 及其化合物 |
结合真实情境中的应用实例或通过实 验探究,了解硫及其重要化合物的主要性质,认识这些物质在生产中的应用和对生态环境的影响。 |
能从物质类别、元素价态的角度,依 据氧化还原原理说明物质的转化路径。 |
|
物质性质及 物质转化的 价值 |
结合实例认识金属、非金属及其化合物 的多样性,了解通过化学反应可以探索 物质性质、实现物质转化,认识物质及 其转化在促进社会文明进步、自然资源综合利用和环境保护中的重要价值。 |
能说明常见元素及其化合物的应用 (如金属冶炼、合成氨等)对社会发 展的价值、对环境的影响。能有意识运用所学的知识或寻求相关证据参 与社会性议题的讨论(如酸雨和雾霾防治、水体保护、食品安全)。 |
|
学生 必做实验 |
化学反应速率的影响因素 |
能运用变量控制的方法探究影响化 学反应速率的因素,能初步解释化学 实验和化工生产中反应条件的选择问题。 |
本单元学习主要促进学生“宏观辨识与微观探析”“变化观念与平衡思想”“证据推理与模型认知”“科学探究与创新意识”和“科学态度与社会责任”等方面的化学学科核心素养的发展。本章的学科核心素养要求如下:
■ 知道化学变化需要一定的条件并遵循一定规律;认识化学反应速率和限度;能从化学反应速率、化学平衡等角度,认识和调控化学反应。
■ 运用变量控制、定量实验等方法研究化学反应,提出问题和假设、设计实验方案、组装实验仪器,与同学合作完成实验,客观地记录现象和数据,并基于现象和数据分析得出结论。
■ 运用化学反应原理来讨论和解决与化工生产相关的实际问题,形成节约资源、保护环境的可持续发展意识。
3. 单元结构
本单元主要包括“化学反应速率及其影响因素 ”;“可逆反应、化学平衡 ”;“ 以硫酸工业为例的化工生产”等,主要内容的知识结构如图 1 所示:
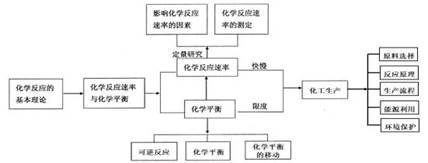
图 1 “化学反应速率和化学平衡”单元教学内容的知识结构
二、教学内容分析
1. 教学内容
本课时“影响化学反应速率的因素”教学主要内容是引导学生认识化学反应速率与反应物自身性质密切相关,进而引出外界因素对同一反应的反应速率影响问题。通过控制变量实验与推理探究固体颗粒大小、浓度、温度、催化剂、压强对化学反应速率的影响。
2. 地位作用
本课时通过实验探究活动和学生熟悉的反应实例分析,认识化学反应速率和化学平衡移动的影响因素,为后续选择性必修阶段进一步从定量的角度深入学习化学反应速率、化学平衡移动以及化工生产工艺设计奠定基础。
三、学生学情分析
1. 学生的相关学习经验
初中阶段学生对化学反应的快慢和进行程度具有初步的感性认识,在必修一中,学生初步完成了氧化还原反应、物质的量以及元素及其化合物等知识的学习,已经具有一定的化学反应速率影响因素的学习与探究能力。
2. 学生可能遇到的学习困难
学生运用控制变量思想设计实验方案的经验存在不足,需要教师多加以引导。压强的影响理解上略有些抽象,且学生的证据推理能力还存在很大的上升空间,需要证据推理与实验展示相结合帮助学生加以理解。
四、教学目标
1.根据实验分析归纳出影响化学反应速率的因素,增强证据推理意识,从微观角度理解浓度和压强对速率影响的关联,发展宏观辨识和微观探析。
2.通过设计实验方案、合作完成实验、基于实验事实得出结论,重温科学探究的一般程序,掌握“变量控制”法,增强科学探究能力。
3.认识化学反应速率是可调控的,形成变化观念,感受控制反应条件在生产和科学研究中的作用,增强对化学学科的应用能力,提升社会责任感。
五、教学重点和难点
1.教学重点
化学反应速率的影响因素及变量控制的实验探究
2.教学难点
实验探究方案的设计
六、教学策略分析
本节课以“如何提高塑料的降解速率”为情境,引导学生完成“影响化学反应速率的因素”的探究,激发学生的学习兴趣,并引导学生解决当前社会面临的环境问题,感悟化学在生产生活中的重要作用。教学中设计实验探究引导学生理解化学反应速率的影响因素,在“探究1固体颗粒大小”后,即提问“为什么选择这个反应进行研究?”,帮助学生理解后续实验方案设计中研究对象的选择。而在“探究2浓度”的实验设计中,学生已能找到适合的研究对象,进而引导学生在实验设计时要注意控制变量,认识“为什么要控制变量”,以及“如何控制变量”。变量控制的实验探究是在逐步引导,多个阶梯式问题中推进的,帮助学生初步学会运用控制变量思想进行实验方案的设计,完成影响化学反应速率因素的相关探究活动。
七、教学过程设计
|
环节 |
教师活动 |
学生活动 |
设计意图 |
|
引入 |
[展示]塑料降解慢导致白色污染的视频。 [提问]如何提高塑料的降解速率? |
思考如何提高塑料降解塑料。 |
联系社会问题,激发学习兴趣。 |
|
环节一: 联系生活 提出假设 |
[展示]生产生活中控制反应快慢的实例。 [提问]通过这些实例,说明影响化学反应速率的因素有哪些? [讲解]对同一反应而言,可调控的这些都是外因,而对不同反应而言,这些反应的反应速率均不相同,所以内因是反应物本身的性质。 |
固体颗粒的大小、浓度、温度、催化剂。 |
联系生产生活中的实例,推测影响化学反应速率的因素,在已有认知基础上构建新知。 |
|
环节二: 实验探究 验证假设 |
内因:反应物的性质 [展示]钠、镁与水反应的视频。 |
认识影响化学反应速率的主要因素是反应物的性质。 |
回顾旧知,理解内因。 |
|
外因1:固体颗粒大小 [展示]实验设计表格 [提问]在上节课已观察不同状态的大理石和同浓度的盐酸反应的实验,这是上节课采用的实验设计表格,所采用的研究方法是什么? [实验1]不同状态的大理石和同浓度的盐酸反应(视频)
[提问]为什么选择这个反应进行研究? 以下两个反应是否适合作为影响化学反应速率的研究对象? 1. HCl+NaOH=NaCl+H2O 2. 2Na+2H2O=2NaOH+H2↑ |
理解研究方法需运用控制变量。 其它条件不变时,减小固体颗粒大小,可以增大反应速率。 研究对象: Ø 有明显的现象 Ø 反应速率适中 Ø 安全、简便 |
根据上节课已完成的固体颗粒大小对反应速率影响实验为基础,得到相应结论,并探讨研究对象和研究方法的确定,为后续实验方案设计做铺垫。 |
|
|
外因2:浓度 [提问]可选择什么研究对象进行研究? 如何设计实验? [实验2]镁和不同浓度的盐酸反应 [提问] 1. 该反应中,增加镁的质量是否能够提高反应速率? 2. 该反应中,增加盐酸的体积是否能够提高反应速率?
[展示]镁投入稀盐酸后速率随时间变化曲线 |
思考、回答。 运用控制变量法设计实验方案。 其它条件不变时,增大反应物的浓度(溶液和气体),可以增大反应速率。 均不能,固体和纯液体不能改变浓度,反应速率与物质的总量无关。 思考曲线变化原因。(前半段温度影响,后半段浓度影响。) |
学会选择合适的研究对象,并运用控制变量的方法设计实验。 通过问题组,认识到浓度对化学反应速率的影响的概念限定。 根据曲线变化,运用浓度影响,推测温度影响。 |
|
|
外因3:温度 [实验3]同浓度的硫代硫酸钠溶液和盐酸在室温、冰水浴条件下反应 [讲解]温度每升高10℃,反应速率可以增大到原来的2~4倍。 |
其他条件不变时,升高温度,化学反应速率增大 。 |
通过学生不熟悉的反应进行实验,学会从多角度观察实验。 |
|
|
外因4:催化剂 [实验4]在双氧水中加入二氧化锰 [讲解]催化剂在工业生产、生物体化学反应、环境保护中都有重要作用。 |
催化剂能大大加快化学反应速率。 |
介绍催化剂的相关知识,认识到催化剂的重要性。 |
|
|
外因5:压强 [提问]压强如何影响化学反应速率?联系浓度对反应速率的影响。 [提问]这次验证猜想的实验研究对象,应该具有什么特点? [实验5]硫化氢气体和二氧化硫气体混合,增大压强 |
压强增大,压缩容器,浓度增大,反应速率增大。 反应物有气体参与。 得出压强对化学反应速率的影响结论。 |
从微观角度理解浓度和压强对速率影响的关联,提升宏微结合的分析能力。 |
|
|
环节三: 归纳总结 提升主题 |
[小结] 1.带领学生总结影响化学反应速率的内因与外因。 2.用化学反应速率的知识解释生产生活问题。 3.尝试说出提高塑料降解速率的方法。 |
总结整理,思考回答。
|
感受化学与生产生活的密切联系,感受学科价值。 |
【板书设计】
影响化学反应速率的因素
一、内因:反应物本身性质 (主要因素)
二、外因:(次要因素)
1. 固体颗粒大小
2.浓度
3.温度
4.催化剂
5.压强
八、课堂学习评价
